近日,我院李兴淑教授团队在治疗缺氧肿瘤的研究上取得重要进展。由于较低的氧气依赖性,I型光敏剂(PS)被认为是光动力疗法(PDT)的更好候选者。然而,由于缺少通用有效的设计策略,I型有机PS的报道相对较少。此外,PS代谢和清除途径是一种重要的药代动力学特征,通过治疗后从体内消除PS来避免潜在的生物毒性(包括皮肤烧伤、皮肤过敏和全身致敏等),但在很大程度上这一特征却被忽视了。因此,构建一个低氧气依赖性的高生物安全性的I型有机PS来增强缺氧肿瘤的治疗仍然是一个巨大的挑战。
针对这些问题,李兴淑教授团队提出了一种基于Förster共振能量转移(FRET)机制的智能分子设计策略,成功开发了一种多功能二元酞菁分子(PcSZ)。PcSZ可以在水溶液中自组装成均匀稳定的纳米粒子(NanoPcSZ)。乏氧条件下,光照NanoPcSZ生成的超氧阴离子(O2·-)的量比在相同条件下光照商用PS亚甲基蓝(MB)高出约2.7倍。并且得益于FRET效应,NanoPcSZ在近红外范围(600-900 nm)内显示出广泛的光谱吸收。一旦暴露在808 nm的光下,NanoPcSZ也表现出产热能力,光热转换效率比商用光热剂吲哚菁绿(ICG)高2.7倍。基于这些独特的特征,NanoPcSZ对4T1细胞具有明显的光细胞毒性,在缺氧环境下,半数最大抑制浓度(IC50)为0.17±0.02 μM,比MB低了55倍。此外,NanoPcSZ在全身给药后表现出优异的肿瘤富集能力,其肿瘤/肝脏富集量比高于6。最终,当NanoPcSZ用于临床前模型的肿瘤光疗时,实现了显著的实体瘤抑制。值得注意的是,NanoPcSZ可以通过肾脏排出,避免了潜在的生物毒性。该研究工作为设计具有高生物安全性的和低氧依赖性的新型有机光敏剂提供新的策略。
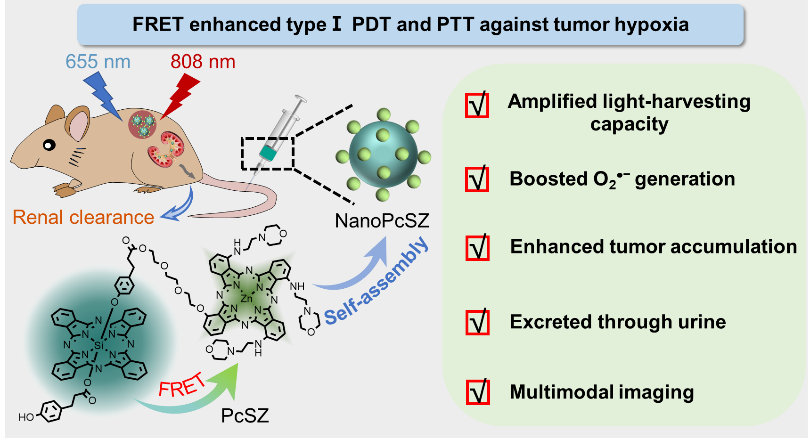
图1 肾脏可清除的自组装纳米光敏剂(NanoPcSZ)介导的I型PDT和PTT增强诊疗的示意图。
成果以“A Renal Clearable Nano-Assembly with Förster Resonance Energy Transfer Amplified Superoxide Radical and Heat Generation to Overcome Hypoxia Resistance in Phototherapeutics”为题发表在Angew. Chem. Int. Ed.上。福州大学化学学院李兴淑教授和韩国梨花女子大学Juyoung Yoon教授为论文的通讯作者,福州大学化学学院博士生赵园园和硕士生张晓君、许毅辉为论文的共同第一作者。该研究得到了国家自然科学基金等经费的资助。
导师介绍
李兴淑,福州大学化学学院教授、博导,国家优秀青年基金获得者、福建省闽江学者特聘教授,入围2023和2024全球前2%顶尖科学家榜单。现任福建省肿瘤转移药物干预重点实验室副主任、福建省免疫学会免疫与转化专业委员会第一届委员会常务委员、福州大学生物化工专业博士学位点负责人以及福州大学化学学院学位评定委员会成员。主要从事基于功能染料分子构建具有疾病治疗与成像检测功能的超分子光敏剂和纳米诊疗剂,研究内容涉及到化学、光子学、生物学和医学等多个学科的交叉领域。迄今,在Nat. Rev. Clin. Oncol.、Chem. Soc. Rev.、J. Am. Chem. Soc.、Angew. Chem. Int. Ed.、Adv. Mater.和ACS Nano等国际著名期刊发表论文40余篇。论文总被引超过9000,12篇入选ESI高被引论文,单篇最高引用超过2000,H因子31。获福建省自然科学优秀学术论文一等奖。课题组经费充足,与韩国、加拿大、美国、新加坡、芬兰等国家的多个课题组保持合作,课题组常年招收药物化学、应用化学、生物化工、制药工程、生物医学工程等相关专业的硕士、博士、科研助理、博士后,待遇优厚,有意向者请发送简历至邮箱:xingshuli@foxmail.com。
原文链接:https://doi.org/10.1002/anie.202411514