近日,我院卢春华/杨黄浩课题组在Journal of the American Chemical Society上在线发表了题为“T Cell “Rejuvenation” Nanovaccine: Enhancing Immunological Memory and Anti-Tumor Responses through Telomere Extension”的研究论文。在本文中,研究团队创新性地利用树突细胞外囊泡的天然机制,开发了一种长效记忆T细胞疫苗(LMT/OT-II)。该疫苗不仅能高效递呈抗原,更能逆转T细胞的衰老状态,为应对免疫衰老及相关疾病提供了新策略。

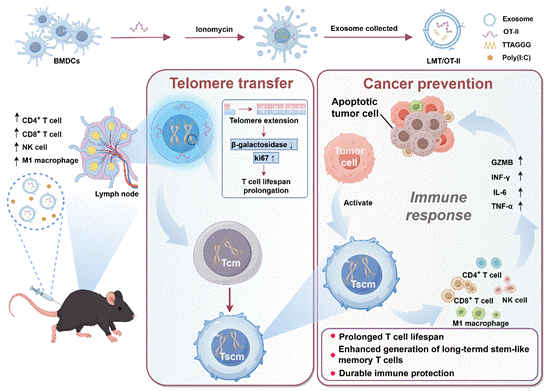
作为疫苗效应的关键执行者,T细胞通过介导细胞免疫和促进抗体生成,建立持久免疫记忆。然而,伴随机体衰老或反复抗原刺激,T细胞端粒持续缩短,导致功能耗竭,难以形成有效免疫防御。如何突破免疫衰老带来的限制,已成为疫苗研发领域亟待解决的关键科学问题。为解决这一问题,研究人员基于骨髓来源树突状细胞(BMDCs)细胞外囊泡(EVs)天然携带端粒组分并可向T细胞完成端粒转移的特性,在其中负载抗原肽,将端粒调控与精准抗原递送有机融合,构建了一种T细胞“逆龄”纳米疫苗。该疫苗的作用核心是利用EV携带的端粒组分实现非端粒酶依赖的端粒转移,延长T细胞端粒并驱动代谢重编程与干细胞样记忆T细胞(Tscm)发生,从而提升T细胞的增殖与效应功能,重塑持久免疫记忆与长期免疫监视。相较传统“抗原+佐剂”模式,该策略在强化抗原呈递的同时逆转免疫衰老,提升应答质量与持续性。以LMT/OT‑II为例,在Poly(I:C)协同下于黑色素瘤模型实现显著肿瘤抑制与生存期延长,并在结肠癌新抗原模型中展现跨适应症通用性。多组学证据一致支持其诱导T细胞功能“年轻化”的分子基础。作为面向免疫衰老的疫苗设计新范式,该平台有望广泛适配肿瘤与病原体抗原,优先惠及老龄及免疫功能低下群体,为构建更通用、有效、持久的免疫干预提供可行路径。
这一成果发表在Journal of the American Chemical Society上,论文的第一作者为福州大学化学学院的博士研究生曹秀萍和医工交叉博士后曾涛,福州大学的卢春华教授、杨黄浩教授为论文的共同通讯作者,为本研究提供了重要的指导。这项研究工作得到了国家重点研发计划以及国家自然科学基金的大力支持。
论文信息:“T Cell “Rejuvenation” Nanovaccine: Enhancing Immunological Memory and Anti-Tumor Responses through Telomere Extension”, Xiuping Cao, Tao Zeng, Shiyan Bai, Shiqing Li, Yana Liu, Liyang Fang, Xiao Fang, Qi Chen, Chunhua Lu, and Huanghao Yang. J. Am. Chem. Soc. 2026, 148, 4706-4721