近日,杨黄浩课题组在阿尔兹海默症治疗方面的研究取得新进展,相关成果以“Dynamic Covalent Peptide-Drug Conjugates Address the Heterogeneity in Alzheimer’s Disease Progression”为题发表在国际顶级期刊Advanced Materials。

阿尔茨海默病(Alzheimer’s disease,AD)在医学研究中被认为是目前最复杂、最难治疗的神经退行性疾病之一。全球老年人群中,大约有10%~30%的人正在受到它的影响,而真正有效的治疗手段仍然非常有限。近年来,美国食品药品监督管理局(FDA)相继批准了三种针对β-淀粉样蛋白(Aβ)的抗体药物——Aducanumab、Lecanemab和Donanemab,用于延缓疾病进展。这被视为AD治疗领域的重要突破。然而,这些药物的临床试验对象,仅限于轻度认知障碍或轻度痴呆患者,因此它们是否同样适用于数量更为庞大的中晚期患者,仍然存在争议。事实上,AD并不是一种静态的疾病,而是一种动态的、进行性的疾病。不同患者之间,疾病发展的速度、阶段和主要病理特征可能截然不同。如果仅仅依据某一个时间点的病理指标,或者依据某一类患者的临床数据来制定给药剂量,就会在真实的治疗场景中面临用药错误或治疗失败的风险。虽然在理论上可以通过大数据分析,对患者进行精细分层,并为不同人群匹配专属的治疗方案,但会不可避免地导致治疗流程复杂化,诊断和随访成本增加,以及预后负担加重。针对上述挑战,构建一种能够追踪疾病进展并自主调节给药方案的药物递送系统,可能有助于将治疗反应的个体差异和医疗资源消耗最小化。
基于生物标志物定义的AD进展轨迹,本研究开发了一种能够解码疾病进展过程中三个关键生物标志物(Aβ、活性氧和葡萄糖)时空演化模式的抗AD纳米治疗剂(CPKNAs),旨在使治疗药物能够随疾病的发展自适应地调节体内分布模式和暴露剂量,以应对AD进展异质性所造成的药效差异。该纳米治疗剂由一种基于动态苯硼酸酯连接的KLVFF肽-姜黄素偶联物自组装而成。在体外模拟AD生物标志物时间演变的病理环境中,CPKNAs中的动态共价键经历了不同程度的水解、氧化分解和竞争结合,展现出分层级的药物释放行为。这种独特的特性使CPKNAs能够区分不同的疾病进展阶段,并在特定的病变中精细地滴定姜黄素剂量。为了全面评估该纳米治疗剂对抗AD异质性进展的潜力,该研究使用了7种具有不同程度病理负荷的细胞模型和3种模拟不同疾病阶段的转基因小鼠,系统地验证了CPKNAs能够在统一的给药方案下,有效地阻止AD病理进展,重塑脑微环境,改善记忆和认知缺陷。
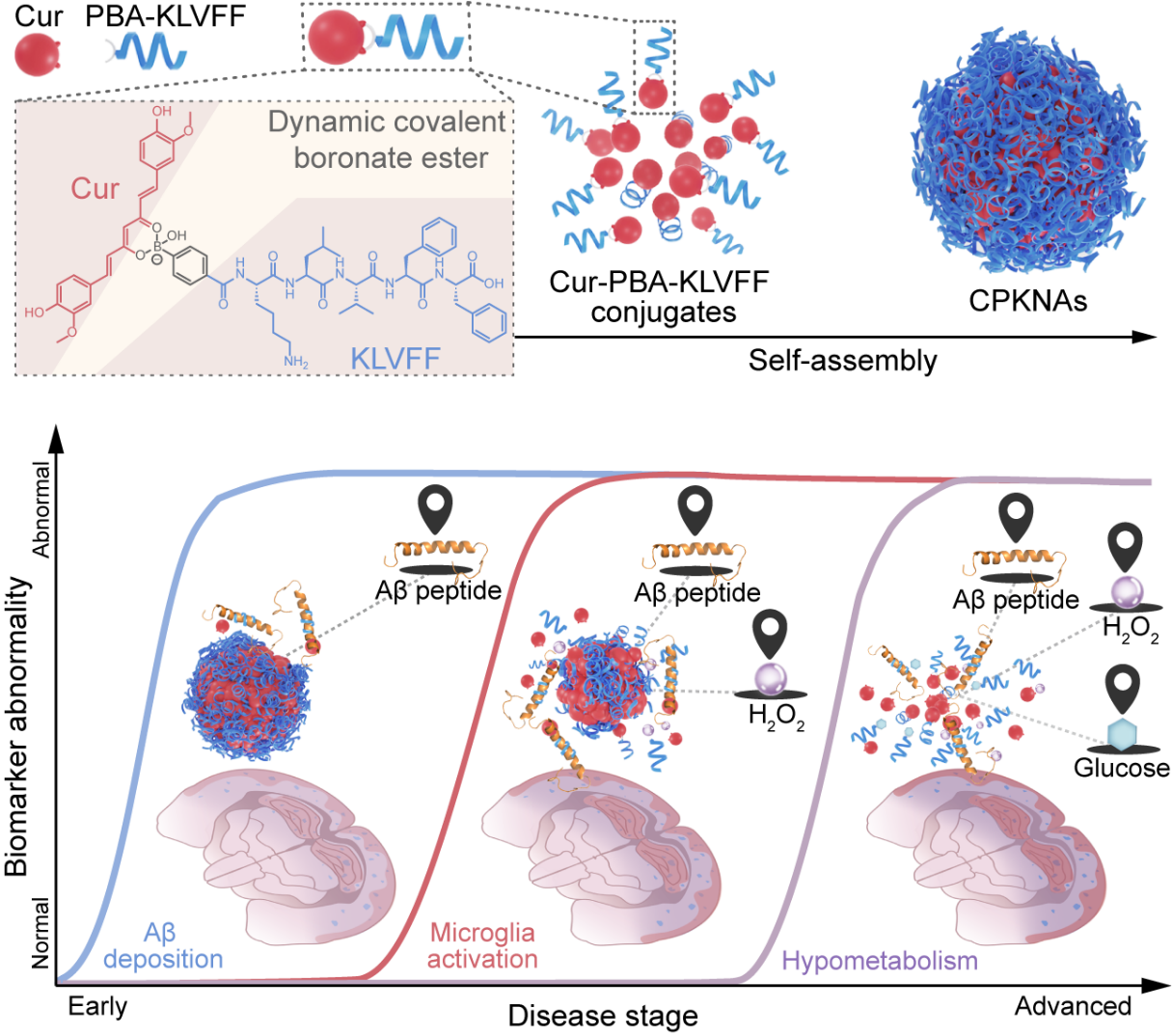
图 1 由动态苯硼酸酯连接的肽-药物偶联物衍生的纳米治疗剂(CPKNAs)通过追踪与AD疾病进展阶段相关病理信号的时空坐标自主调节脑内药物的分布和剂量的机理示意图。
福州大学化学学院杨黄浩教授、陈兆委教授与深圳先进研究院陈支通研究员为论文的共同通讯作者,福州大学化学学院2022级博士研究生杨宇恒为第一作者。该研究得到了国家自然科学基金以及新基石科学基金会的支持。
论文信息
“Dynamic Covalent Peptide-Drug Conjugates Address the Heterogeneity in Alzheimerʼs Disease Progression.” Yuheng Yang, Ting Wu, Xuan Fan, Yuhang Yao, Chen Chen, Kun Kang, Xianzhe Tang, Tingjing Huang, Yixuan Xu, Yu He, Zhitong Chen,* Zhaowei Chen,* Huanghao Yang*. Advanced Materials (2026): e16343. DOI: 10.1002/adma.202516343.